💡
原文中文,约5300字,阅读约需13分钟。
📝
内容提要
为理解生命过程的分子机制,需解析生物大分子的三维结构。冷冻电镜和X射线晶体学是主要技术,AlphaFold等计算方法也取得进展。卡内基梅隆大学提出的AQuaRef方法结合机器学习和量子精修,提升了蛋白质结构的精确度,已在《Nature Communications》发表。
🎯
关键要点
- 理解生命过程的分子机制需要解析生物大分子的三维结构。
- 冷冻电镜和X射线晶体学是主要的实验技术,AlphaFold等计算方法也取得了进展。
- 卡内基梅隆大学提出的AQuaRef方法结合机器学习和量子精修,提升了蛋白质结构的精确度。
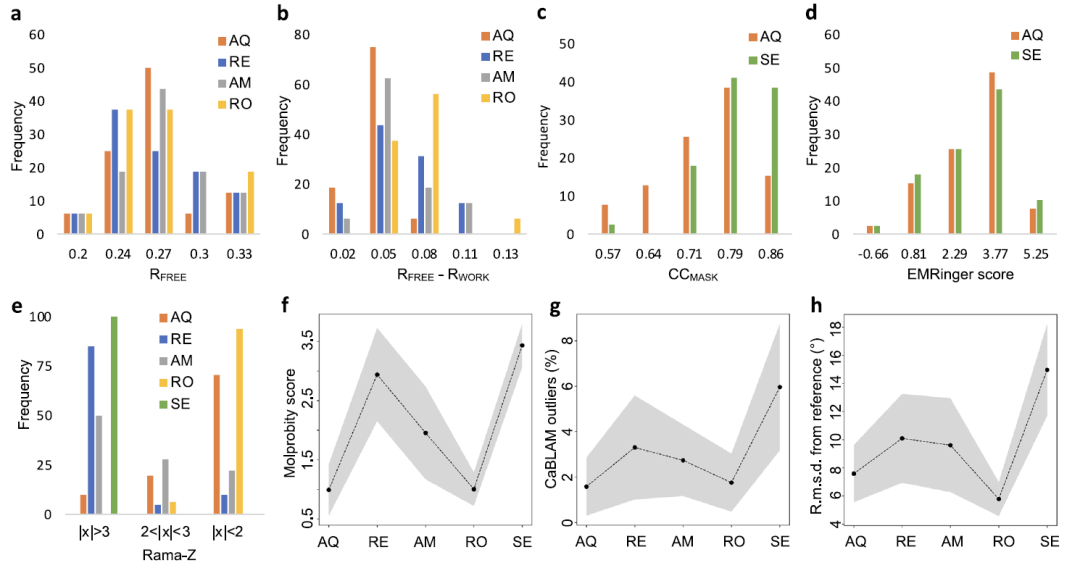
- AQuaRef在61个低分辨率模型中表现优于57个模型,且无需人工干预即可确定质子位置。
- 研究团队构建了覆盖化学组成、构象空间和分子间相互作用的100万样本数据集。
- AQuaRef通过主动学习策略优化样本,最终获得约100万条样本构成的训练集。
- AQuaRef在精修过程中考虑了晶胞对称性及周期性相互作用。
- AQuaRef的量子精修方法在几何质量上优于传统约束方法,且过拟合程度最低。
- AQuaRef在短氢键体系的测试中表现出色,能够恢复与实验数据一致的结构。
- 量子力学方法与机器学习势函数的结合为生物大分子结构精修提供了新的技术路径。
❓
延伸问答
AQuaRef方法的主要创新点是什么?
AQuaRef方法结合了机器学习和量子精修,首次实现全蛋白质原子模型的量子精修,提升了蛋白质结构的精确度。
AQuaRef在低分辨率模型中的表现如何?
在61个低分辨率模型的测试中,AQuaRef在57个模型中表现优于其他方法,且无需人工干预即可确定质子位置。
AQuaRef如何处理氢键和质子位置?
AQuaRef能够在短氢键体系中准确恢复质子位置,与实验数据一致,避免了传统方法的偏差。
AQuaRef的训练数据集是如何构建的?
研究团队构建了覆盖化学组成、构象空间和分子间相互作用的100万样本数据集,以支持机器学习势函数的训练。
AQuaRef与传统精修方法相比有什么优势?
AQuaRef在几何质量上优于传统约束方法,且过拟合程度最低,能够更合理地恢复结构。
AQuaRef的研究成果发表在哪个期刊上?
AQuaRef的研究成果已发表于《Nature Communications》。
➡️

